9月13日,世界卫生组织宣布,巴伐利亚北欧公司MVA-BN疫苗成为首款被列入世界卫生组织疫苗预认证清单的猴痘疫苗。
世界卫生组织疫苗预认证清单(WHO Prequalification of Vaccines)是世界卫生组织(WHO)制定的一项程序,旨在确保用于国际采购的疫苗符合质量、安全性和有效性标准。该清单用于帮助联合国机构(如,联合国儿童基金会)和各国政府在选择疫苗时,确保所选疫苗符合国际认可的标准。
简而言之,MVA-BN疫苗成为首款被世界卫生组织认证且推荐各国采购接种的猴痘疫苗。
根据世界卫生组织提供的现有数据,暴露前,接种一针次的MVA-BN疫苗预防猴痘的有效率估计为76%,接种两针次的MVA-BN疫苗预防猴痘的有效率估计为82%。
不过在暴露后接种MVA-BN疫苗预防猴痘的效果不如暴露前接种。此外,该部分没有明确的数据。
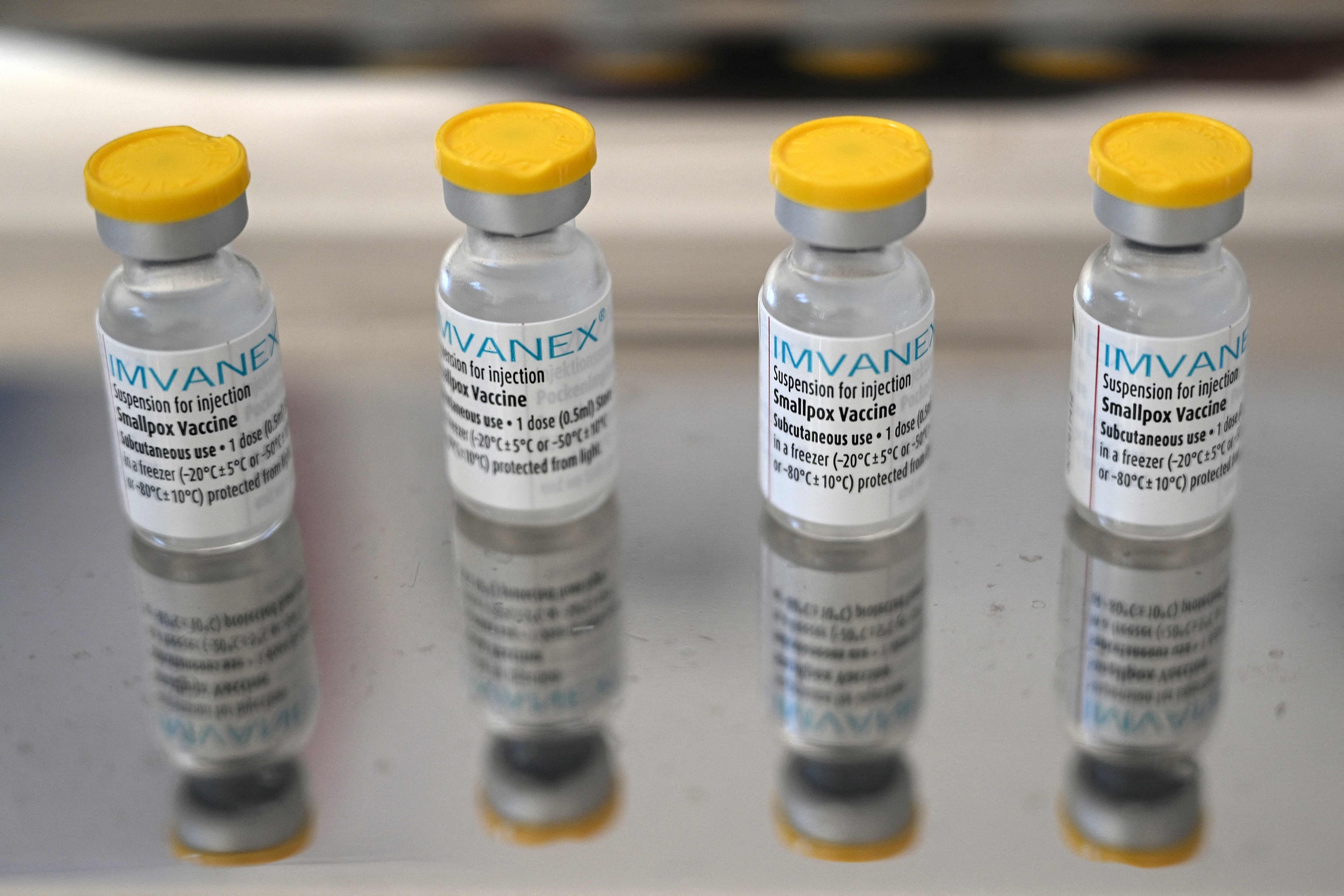
根据世界卫生组织的新闻稿,MVA-BN疫苗用于18岁以上人群接种,按照标准的接种方案需间隔4周进行两剂注射。而在疫苗供应紧张地区,世界卫生组织也推荐单针次接种疫苗。
此外,根据世界卫生组织的新闻稿,在猴痘疫情爆发地区,MVA-BN疫苗疫苗可能可以超适应症用于婴儿、儿童、青少年,以及孕妇和免疫功能低下者。世界卫生组织表示,在这种情况下,猴痘疫苗接种的潜在收益大于潜在的风险。
世界卫生组织总干事谭德塞表示,这是首个针对猴痘疫苗的预认证,是抗击该疾病的重要一步。“我们现在需要紧急扩大采购、捐赠和推广,以确保疫苗能公平地到达最需要的地方。”
值得注意的是,猴痘疫情已两次被世界卫生组织宣布构成“国际关注的突发公共卫生事件”。两次猴痘疫情“警报拉响”都源于刚果。
8月14日,世界卫生组织总干事谭德塞宣布,猴痘疫情构成“国际关注的突发公共卫生事件”。此前,世界卫生组织宣布猴痘构成“国际关注的突发公共卫生事件”的时间区间为2022年7月23日至2023年5月11日。
世界卫生组织数据显示,2024年以来报告猴痘病例数超过1.56万例,已超过去年病例总数,其中死亡病例达537例。
据人民日报健康客户端不完全统计,截至8月31日,全球至少已有4款猴痘疫苗在全球各地获批,分别为OrthopoxVac、MVA-BN、LC-16、ACAM2000,这四种疫苗原本均是用于预防天花而被研发。
据世界卫生组织新闻稿,其中,LC-16和ACAM2000也正排队等待审核进入世界卫生组织预认证和紧急使用清单。此外,还有6款猴痘诊断产品等待申请紧急使用清单。
截至目前,我国尚无猴痘疫苗产品上市。2023年9月20日起,国内将猴痘纳入乙类传染病管理,采取乙类传染病的预防、控制措施,也就是与新冠、非典、艾滋病、病毒性肝炎等传染病同级别管理。
9月9日,国药集团中国生物上海生物制品研究所自主研发的MVA株猴痘减毒活疫苗获得国家药品监督管理局签发的临床试验通知书,这是我国首款获批临床的猴痘疫苗。据中国生物上海生物制品研究所介绍,此次获批临床的猴痘减毒疫苗是基于复制缺陷型痘苗病毒MVA株开发,该疫苗株的安全性、有效性已得到充分的临床数据论证。
国内多家体外诊断(IVD)公司也已研发猴痘检测试剂盒。据国金证券研报,截至2022年7月24日,国内已有100家医药企业共137款猴痘检测盒获得欧盟CE认证。其中,之江生物、硕世生物、达安基因、圣湘生物等公司已获得海外订单。




还没有评论,来说两句吧...